CNRS - Une piste innovante dans l'AVC : cibler la matrice qui entoure et sert de support aux cellules cérébrales
AVC : prévenir les séquelles en agissant sur l'environnement des neurones ?
- Théragora le 15 novembre 2018 / CNRS N° 15 - Page 0 - crédits iconographique © Xavier Laffray / CRRET
Pour protéger les neurones et limiter les séquelles suite à un AVC, des chercheurs du CNRS, de l'Université de Caen Normandie, de l'Université Paris-Est Créteil ainsi que de la société OTR3 ont suivi une piste innovante : cibler la matrice qui entoure et sert de support aux cellules cérébrales. Leurs résultats, qui viennent d'être publiés dans la revue Theranostics, valident cette stratégie chez le rat et conduiront à une étude clinique d'ici fin 2019.
Avec plus de 300 cas par jour en France, les accidents vasculaires cérébraux (AVC) sont la première cause de handicap acquis chez l'adulte et la deuxième cause de mortalité. 80 à 85 % sont dus à l'occlusion d'une artère cérébrale par un caillot sanguin (AVC ischémique) : alors privés de leur alimentation en oxygène, les neurones à proximité meurent. Le seul traitement existant consiste à éliminer ce caillot, ce qui n'est possible que dans les premières heures de l'AVC et ne permet donc de traiter qu'une minorité de patients. Par ailleurs, les lésions cérébrales peuvent persister et s'aggraver longtemps après le début de l'AVC et aucun traitement n'est encore disponible pour les freiner ou pour améliorer la récupération fonctionnelle.
De nombreuses pistes de recherche étudient des moyens de protéger les neurones de cette dégénérescence. Mais les traitements s'attaquant à la dégénérescence n'ont connu que des échecs cliniques, ce qui a poussé l'équipe de la chercheuse CNRS Myriam Bernaudin à s'intéresser à un domaine peu exploré : l'environnement des cellules, ou matrice extracellulaire. La matrice, qui sert de support aux cellules et abrite des facteurs de croissance, se retrouve en effet désorganisée à la suite d'un AVC, ce qui amplifie la mort neuronale. L'équipe du laboratoire Imagerie et stratégies thérapeutiques des pathologies cérébrales et tumorales (CNRS/UNICAEN/CEA) s'est donc rapprochée de collègues spécialistes de la matrice extracellulaire, au laboratoire Croissance, réparation et régénération tissulaires (CNRS/UPEC), et de la société de biotechnologies OTR3, qui a déjà mis sur le marché des traitements de « thérapies matricielles » pour la cicatrisation d'ulcères cutanés ou de cornée.
Les chercheurs ont montré, chez le rat, l'efficacité de cette nouvelle approche pour protéger le cerveau et améliorer la récupération fonctionnelle à la suite d'un AVC ischémique. L'injection intraveineuse d'un agent qui mime certains composants structurants de la matrice extracellulaire, les héparanes sulfates, a permis de protéger et de reconstituer cette matrice, de favoriser le développement de nouveaux neurones et la régénération des vaisseaux sanguins, et d'améliorer la récupération des fonctions sensorielles et motrices.
Il s'agit donc d'une piste prometteuse pour limiter les séquelles de l'AVC, qui viendrait en complément des techniques existantes d'élimination du caillot sanguin. Des essais cliniques pilotes devraient démarrer d'ici fin 2019.
Ces recherches ont été soutenues par le CNRS, l'Agence nationale de la recherche, l'Université de Caen Normandie et la région Normandie. Le développement clinique sera assuré avec la société OTR3 qui a reçu le soutien de la Commission européenne avec un financement H2020 SME (n° 811729).
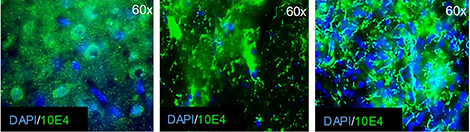 La matrice extracellulaire (marquée en vert) entoure les cellules cérébrales (noyaux marqués en bleu). A gauche, chez des animaux normaux. Au milieu, après un AVC chez des animaux non traités, la matrice est disloquée et les cellules cérébrales dégénèrent. A droite, chez des animaux qui ont été traités après un AVC, l'organisation de la matrice est rétablie et les cellules sont préservées. © Xavier Laffray / CRRET |
Références
A heparan sulfate-based matrix therapy reduces brain damage and enhances functional recovery following stroke, Yacine Khelif, Jérôme Toutain, Marie-Sophie Quittet, Sandrine Chantepie, Xavier Laffray, Samuel Valable, Didier Divoux, Fernando Sineriz, Emanuelle Pascolo-Rebouillat, Dulce Papy-Garcia, Denis Barritault, Omar Touzani*, Myriam Bernaudin*. Theranostics, 12 novembre 2018. DOI : 10.7150/thno.28252
* Contribution équivalente.










